2026 年 2 月 24 日,北京大学第三医院呼吸与危重症医学科双聘教授、北京大学未来技术学院邱义福教授团队联合孙永昌教授团队,在Nature Communications发表题为 “DNA-PK-mediated phosphorylation of STAT6 establishes a non-canonical type 2 immunity axis to prevent macrophage senescence” 的研究论文。该研究揭示了调控巨噬细胞衰老的DNA-PK/STAT6/PU.1非经典2型免疫分子轴,首次在体内模型与临床样本中证实该通路异常与肺纤维化、慢阻肺病(COPD)的发生发展密切相关,为衰老相关慢性呼吸疾病的靶向干预提供了关键理论依据与潜在分子靶点。
炎性衰老作为个体衰老进程中免疫系统功能失调的核心产物,是多种慢性退行性疾病的核心病理基础。其中巨噬细胞作为固有免疫的核心效应细胞,其功能紊乱、组织慢性炎症与修复能力失衡,已被证实是慢阻肺病、肺纤维化等难治性慢性呼吸疾病发生发展的关键驱动因素。邱义福团队前期研究明确了2型细胞因子IL-4介导的信号通路在巨噬细胞衰老与DNA修复调控中发挥核心作用,但其上下游分子机制,尤其是该通路在呼吸系统衰老相关疾病中的病理生理功能尚不清楚。
该研究系统解析了DNA损伤压力下巨噬细胞内的非经典2型免疫调控通路,发现DNA损伤应答核心激酶DNA-PK可直接与IL-4通路核心效应分子STAT6发生相互作用,特异性催化STAT6 Ser807位点发生磷酸化修饰。该修饰独立于STAT6经典 Tyr641磷酸化激活途径,通过抑制STAT6与E3泛素连接酶RNF128的结合,阻断其泛素-蛋白酶体降解途径,显著提升活化形式STAT6的蛋白稳定性;稳定后的STAT6可进一步招募髓系细胞特异性转录因子PU.1形成转录复合物,协同激活下游DNA修复基因的转录,最终实现对巨噬细胞衰老的有效抵御。
为明确该调控轴在呼吸系统衰老相关疾病中的病理生理意义,研究团队构建了STAT6 S807A(不可磷酸化突变)与STAT6 S807E(模拟持续磷酸化突变)基因敲入小鼠模型。体内实验结果显示,STAT6 S807E突变小鼠的巨噬细胞呈现出显著增强的DNA损伤修复能力与抗衰老表型;在博来霉素诱导的肺纤维化小鼠模型中,该突变可有效缓解小鼠肺组织纤维化进程,直接证实了STAT6 Ser807磷酸化修饰对肺纤维化的关键保护作用。
在临床转化层面,研究团队针对慢阻肺病患者临床样本的分析进一步验证了该通路的疾病相关性。结果发现慢阻肺病患者肺组织中的人源STAT6 Ser817位点(对应鼠源Ser807)磷酸化水平显著下调,且该位点的磷酸化水平与细胞衰老标志物的表达水平呈显著负相关。这一临床证据明确提示,DNA-PK/STAT6/PU.1调控轴的功能异常可能是人类慢阻肺病发生发展的重要分子机制,同时也为该病的早期筛查提供了潜在生物标志物,为探索精准干预策略提供了全新靶点。
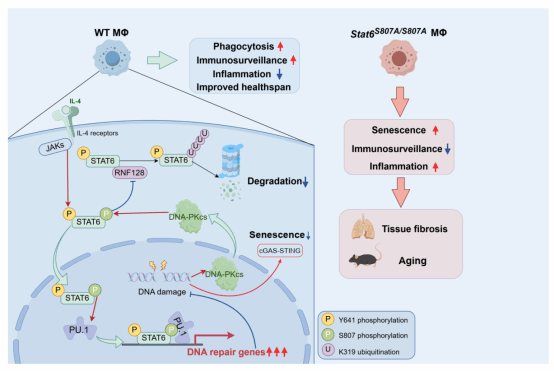
图1:DNA-PK/STAT6/PU.1分子轴调节巨噬细胞DNA修复与衰老
该研究首次鉴定出STAT6 Ser807磷酸化是调控巨噬细胞衰老与肺组织稳态的关键分子开关,完整填补了IL-4非经典2型免疫信号通路的机制空白(图1)。尤为重要的是,研究将固有免疫细胞的衰老调控机制与慢阻肺病、肺纤维化等高发、难治性慢性呼吸疾病深度关联,为开发靶向巨噬细胞衰老的治疗新策略奠定了坚实的理论基础。
北京大学未来技术学院周炤博士为论文第一作者,邱义福教授、吴冬梅博士、北京大学第三医院孙永昌教授为论文共同通讯作者。北京大学第三医院呼吸与危重症医学科、北京大学流式平台与光学平台、清华大学蛋白质组学平台为研究提供了重要技术支持。
原文链接 Nat Commun 2026 Feb 24. PMID:41735318 DOI: 10.1038/s41467-026-69996-8
 科室动态
科室动态