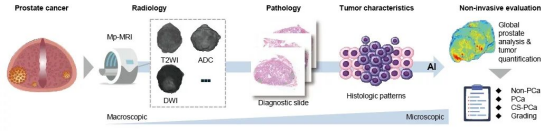
随着人工智能等新兴技术的快速发展,影像学数据与病理学结果之间的关联研究迎来了新的视角,开启了无创精准诊断与分级的广阔前景。近期,北京大学第三医院泌尿外科张树栋团队、上海长征医院任善成团队、南京医科大学第一附属医院李杰团队(江苏省人民医院)、北京友谊医院、青岛大学附属医院和安徽大学邵立智团队、重庆邮电大学、清华大学、香港理工大学等算法团队开展的医工交叉研究,在国际顶尖医学期刊《Nature Cancer》(IF=28.5)发表了题为《An MRI-Pathology Foundation Model for Non-Invasive Diagnosis and Grading of Prostate Cancer》的高质量研究成果。研究团队针对前列腺癌无创诊断和分级的临床需求,在多中心真实患者数据的基础上开发了一个端到端的人工智能(AI)影像-病理基础模型,用于辅助前列腺癌的临床诊断和分级。

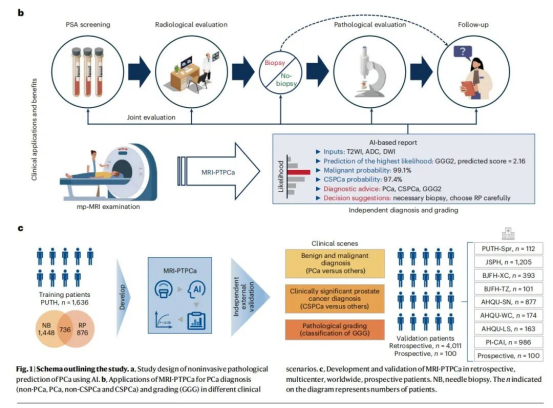
为实现这一目标,研究团队招募了多个中心的回顾性和前瞻性患者队列(共5747名患者),并收集了影像学、病理学和临床检查数据。AI模型的评估方法包括时间外部测试、空间外部测试、人口外部测试以及前瞻性测试。为减少图像序列遗漏、过拟合和仪器差异对结果的影响,团队使用了1,296,950对影像数据进行模型训练,并融合了自监督学习、任务多重学习、Transformer以及基础模型迁移学习等技术,以优化训练过程。
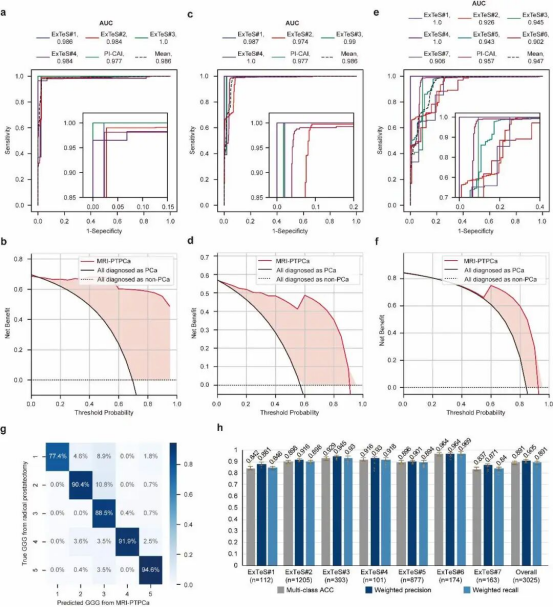
从临床应用角度来看,MRI-PTPCa作为独立的诊断和分级工具,能够有效减少临床实践中的观察者内和观察者间的变异性。该工具可以单独使用,也可以与PSA联合使用,从而解决PSA筛查中较高假阳性率的问题。此外,MRI-PTPCa显著减轻了PSA灰区中诊断的模糊性。在临床显著前列腺癌(CSPCa)的放射学评估中,临床实践通常更注重灵敏度,而不是特异性,以确保更多患者接受病理级评估,从而减少漏诊的风险。然而,这种方法可能会导致不必要的针吸活检,增加医疗资源的负担并导致医源性损伤。MRI-PTPCa显著提高了特异性,同时保持较高的灵敏度,减少了近90%的过度诊断CSPCa的病例。此外,该模型为PI-RADS评分为3的患者提供了可靠的诊断支持,减少了针吸活检后的升降级率,这对于涉及饱和活检、MRI靶向活检、融合活检等增强评估方法的临床评估尤为重要。
MRI-PTPCa在多个临床应用场景中表现出巨大的潜力。研究团队还评估了不同经验水平的放射科医生,探讨AI辅助诊断对临床工作的影响。无论作为平行系统还是预警系统,MRI-PTPCa都能有效提高非侵入性评估的准确性和效率。尽管放射科医生对AI的接受度存在差异,但所有参与者在整合MRI-PTPCa后,都展现出了性能的提升。尤其是初级放射科医生,相较于高级放射科医生,表现出更高的AI接受度,并在诊断准确性和效率上取得显著进展。作为独立系统,MRI-PTPCa在回顾性和前瞻性测试中的表现均超越了放射科医生的基线水平。尽管AI预测模型在伦理和法律方面依然面临挑战,但MRI-PTPCa展现了其在临床实践中的巨大潜力。无论作为独立诊断工具还是辅助系统,它为提高诊断性能提供了有力的解决方案。这些发现为AI在临床实践中的分阶段实施提供了有力的支持,展示了其灵活性,并增强了AI向临床转化的信心。
这一最新成果的取得,建立在北医三院团队长期深耕“人工智能+前列腺癌”领域的持续探索之上。事实上,早在2021年和2020年,该团队就已在国际权威期刊上连续发表系列研究成果,为今日的突破奠定了坚实基础。
Reference: Shao, L., Liang, C., Yan, Y. et al. An MRI–pathology foundation model for noninvasive diagnosis and grading of prostate cancer. Nat Cancer (2025).
Cancers
基于MRI定量影像组学特征的深度学习模型预测前列腺癌术后复发
2021年,《Cancers》杂志刊发了北医三院泌尿外科与国内外多家机构合作的研究成果,题为《Deep Learning with Quantitative Features of Magnetic Resonance Images to Predict Biochemical Recurrence of Radical Prostatectomy: A Multi-Center Study》。该研究针对前列腺癌根治术后患者生化复发(BCR)风险预测难题,创新性地提出了深度影像组学预测模型(DRS-BCR)。
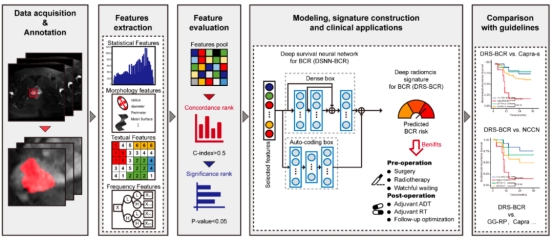
该研究共纳入来自三家医院的485例患者,严格按照标准进行随访与复发界定。团队基于T2加权MRI提取702个定量影像特征,并结合深度生存神经网络进行建模。结果显示,DRS-BCR模型在多中心验证队列中的C-index达到0.802,显著优于CAPRA-S评分(0.677)、NCCN模型(0.586)及Gleason分级(0.583)。
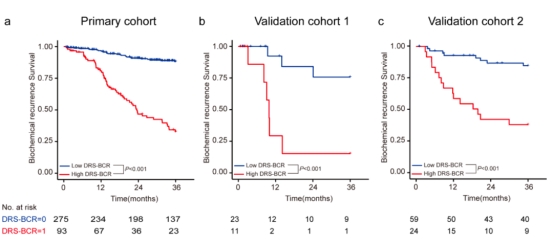
临床应用分析表明,该模型能够有效避免近三分之一患者因传统风险评估不足而面临的过度治疗,为早期识别高风险复发人群提供了重要依据。通过该模型,医生能够在患者术前或术后尽早识别高风险群体,从而在最佳窗口期开展新辅助或辅助治疗,提升长期肿瘤学控制率。这一研究不仅验证了MRI影像组学在复发预测中的潜力,也推动了精准治疗策略的优化。
Reference: Yan, Y.; Shao, L.; Liu, Z.; et al. Deep Learning with Quantitative Features of Magnetic Resonance Images to Predict Biochemical Recurrence of Radical Prostatectomy: A Multi-Center Study. Cancers 2021, 13, 3098.
Theranostics
人工智能模拟放射科诊断行为,减少活检与术后病理不一致
更早在2020年,北医三院泌尿外科团队与合作伙伴在国际期刊《Theranostics》发表了题为《Radiologist-like artificial intelligence for grade group prediction of radical prostatectomy for reducing upgrading and downgrading from biopsy》的研究成果,首次尝试利用人工智能模拟放射科医生的诊断行为,以解决活检病理与术后病理常见的不一致问题。
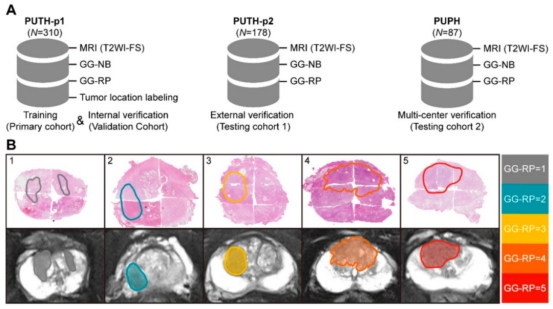
在该研究中,团队纳入575例患者,开发了基于深度强化学习的前列腺癌分级预测框架PCa-GGNet。该模型能够自动搜索关键MRI切片,进行患者层面的病理分级预测。结果显示,PCa-GGNet在预测根治术后病理Gleason分级时,准确率达到0.815,远高于穿刺活检的0.437。更为重要的是,该模型显著降低了活检与术后病理的升降级比例,升高率下降27.9%,降低率下降6.4%,在减少过度治疗和避免漏治方面具有重大意义。
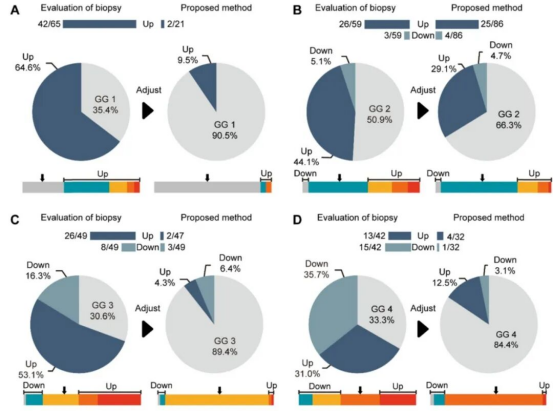
这一成果不仅展示了深度强化学习在医学影像中的应用潜力,更为临床路径优化提供了全新工具。通过模拟放射科医生的诊断流程,AI有望帮助医生在手术前获得更接近真实病理的分级信息,从而提升治疗决策的准确性。
Reference: Shao, L., Yan, Y., Liu, Z.et al. (2020). Radiologist-like artificial intelligence for grade group prediction of radical prostatectomy for reducing upgrading and downgrading from biopsy. Theranostics, 10(22), 10200-10212.
系列成果的整体意义
从2020年至2025年,北医三院泌尿外科团队携手国内外合作伙伴,围绕前列腺癌的诊断、分级与预后预测,形成了一个递进式的研究链条:
通过深度强化学习(2020),减少活检与术后病理差异,提高分级准确性;
通过影像组学与深度学习(2021),实现术后复发风险的精准预测;
通过MRI-病理基础模型(2025),突破无创诊断与分级的国际难题。
这一系列研究连续发表于《Theranostics》《Cancers》《Nature Cancer》等国际权威期刊,展现了北医三院泌尿外科在人工智能与泌尿肿瘤学交叉领域的持续引领作用。未来,团队将继续推动人工智能在临床中的深度应用,助力前列腺癌诊疗的全流程智能化与个体化发展。
文图丨颜野
审核丨颜野、张树栋
编辑丨董靖晗

 教学科研
教学科研