2026年3月31日,北京大学第三医院医学创新研究院毛凤彪研究员/乔杰院士团队,联合赵晓璐/刘强副研究员于Nature Communications(《自然—通讯》IF: 15.7)发表题为“The landscape and regulatory potential of eccDNAs in mammalian preimplantation embryos”(哺乳动物早期胚胎发育中的eccDNA图谱及其调控潜能研究)的研究成果。

论文截图
染色体外环状DNA(eccDNA)广泛存在于真核生物中,是一类独立于线性染色体的环状DNA分子。其中,长片段(几百kb至数千kb)的环状DNA被称为ecDNA,短片段(数十bp至数千bp)的则统称为eccDNA或microDNA。
近年来,ecDNA因其在驱动肿瘤异质性及耐药性中的关键作用而受到广泛关注,与此同时,短片段eccDNA在正常生理及病理条件下也被广泛发现,具有调控基因表达、参与DNA损伤修复等功能。然而,eccDNA在生命起始的早期胚胎发育阶段是否存在、如何形成、发挥何种功能,目前仍知之甚少。
本研究系统解析了eccDNA在哺乳动物早期胚胎中的动态特征与潜在调控机制,不仅有助于理解其在生理条件下的生物学意义,也为探索eccDNA在胚胎发育异常及相关疾病中的潜在功能提供了新视角。
基于此,研究团队对小鼠早期胚胎各关键发育阶段进行了全基因组测序,首次系统描绘eccDNA在早期胚胎发育中的动态景观。分析表明,eccDNA主要来源于转录活跃区域。干预实验显示,抑制转录活性可显著减少eccDNA的生成,而干扰转录-复制冲突(Transcription-replication conflicts, TRC)修复通路则导致eccDNA水平显著上升,提示TRC在其形成过程中发挥关键作用。功能实验进一步表明,携带合子基因组激活(Zygotic genome activation, ZGA)相关基因Mycn和Egfl7调控序列的eccDNA能够显著上调对应靶基因的表达,展现出增强子样的调控潜能。
本研究系统揭示了早期胚胎发育过程中eccDNA的形成机制与动态特征,首次证实了其在早期胚胎基因表达调控中的潜在功能,为解析早期胚胎发育中eccDNA的动态调控机制提供了重要理论依据。
具体来说,研究团队利用多重置换扩增技术(MDA),对小鼠早期胚胎六个关键发育阶段(受精卵至囊胚)进行全基因组测序,发现eccDNA在早期胚胎中广泛存在,并在2细胞期ZGA时期达到峰值。多组学联合分析表明,eccDNA显著富集于转录活跃的染色质区域,并与活性组蛋白标记及RNA聚合酶II结合区域高度重叠。序列特征分析发现,约30%的eccDNA连接位点含有直接重复序列,提示其形成可能依赖微同源末端连接介导的DNA修复机制。机制实验显示,使用α-amanitin抑制胚胎转录活性显著降低了eccDNA的数量和丰度;相反,干扰TRC缓解通路(Fanconi anemia)则导致eccDNA水平升高,表明转录-复制冲突及相关DNA损伤修复过程在eccDNA形成中发挥重要作用。
为进一步探究eccDNA的调控功能,研究团队利用连接酶辅助的小环积累技术(Ligase-assisted minicircle accumulation,LAMA)合成了携带ZGA关键基因Mycn、Egfl7及发育相关基因Emx1调控序列的eccDNA,分别转染至NIH 3T3细胞及显微注射到小鼠合子中。qRT-PCR结果显示,在2细胞期胚胎中,外源过表达合成的eccDNA后处理组目标基因表达水平显著高于随机序列对照组;在NIH 3T3转染细胞中亦观察到类似趋势。上述结果首次证实eccDNA可作为功能性调控元件,参与早期胚胎发育过程中相关基因的表达调控。
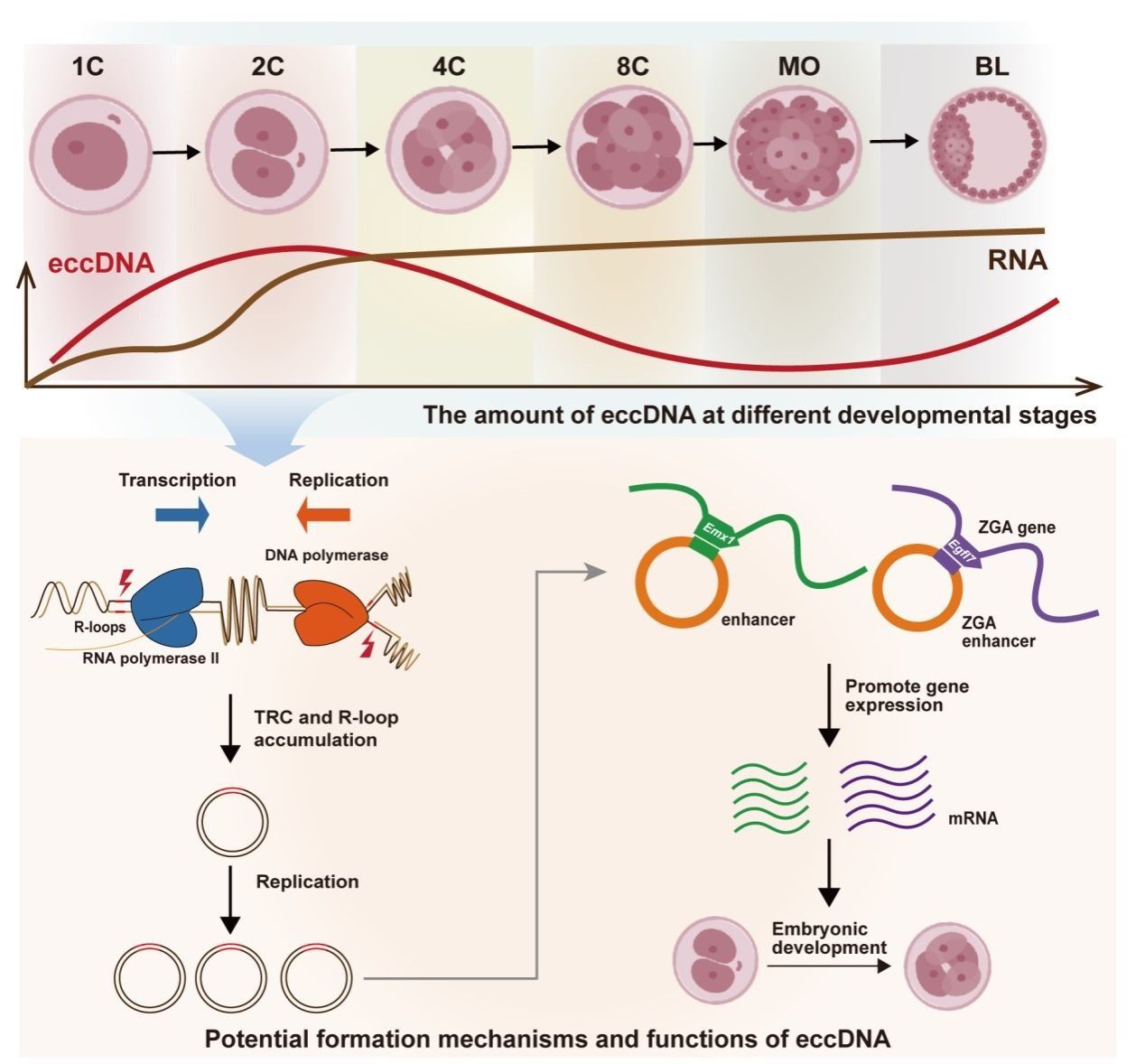
早期胚胎发育过程中eccDNA的形成及作用机制
综上,本研究从聚焦染色体外环状DNA在肿瘤中的促癌功能转向系统解析其在生理条件下的动态特征与调控机制,揭示了eccDNA在哺乳动物早期胚胎发育中的动态图谱,阐明了转录-复制冲突在其形成中的关键作用,并证实了eccDNA作为可移动调控元件参与早期胚胎发育进程。研究为理解eccDNA在生命起始阶段的生物学功能提供了新的视角,不仅有助于深化我们对早期胚胎基因组动态调控机制的理解,也为解决早期胚胎发育障碍和优化辅助生殖策略提供了理论基础和临床指导意义。
北京大学第三医院毛凤彪研究员、赵晓璐副研究员、刘强副研究员和乔杰院士为共同通讯作者;魏玲博士、吴宁博士、陈露博士后为共同第一作者。本研究获得国家自然科学基金、国家重点研发计划、国自然基础科学中心、北京市自然科学基金等项目资助。
原文链接:https://www.nature.com/articles/s41467-026-71227-z